Percée mondiale : une équipe de chercheurs sous la direction du Prof. Dan Peer, l’un des pionniers du développement de médicaments à base d’ARN dans le monde, directeur du laboratoire de nanomédecine et Vice-Président pour la R&D de l’Université de Tel-Aviv, a réussi à détruire la majorité des cellules du myélome multiple, cancer du sang qui apparait dans la moelle osseuse (90 % dans des conditions de laboratoire et 60% dans des tissus prélevés sur des patients), grâce à un médicament à base d’ARN, délivré aux cellules cancéreuses par des nanoparticules ciblantes, qui inhibent leur capacité à se diviser.
 Les résultats de l’étude, réalisée en collaboration avec le Centre médical Rabin (Hôpital Belinson) et menée par la doctorante Dana Tarab-Ravski, ont été publiés dans la prestigieuse revue Advanced Science.
Les résultats de l’étude, réalisée en collaboration avec le Centre médical Rabin (Hôpital Belinson) et menée par la doctorante Dana Tarab-Ravski, ont été publiés dans la prestigieuse revue Advanced Science.
Des résultats très encourageants
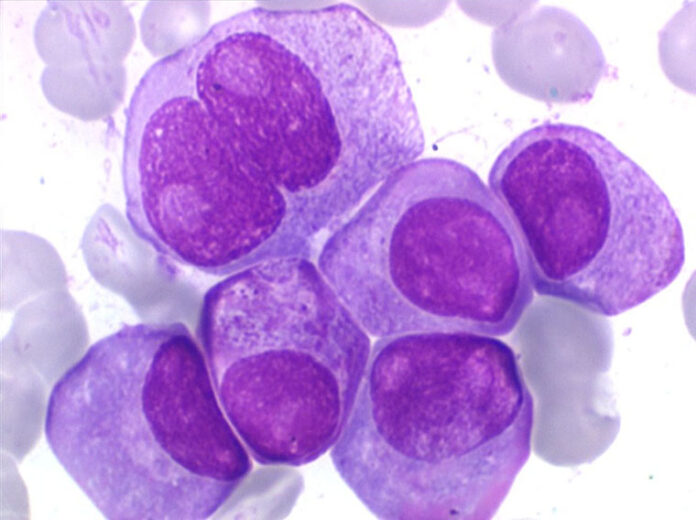
« Le myélome multiple est un cancer du sang qui se développe généralement chez la population âgée », explique Dana Tarab-Ravski. « Contrairement à la plupart des leucémies qui apparaissent dans la circulation sanguine ou les ganglions lymphatiques et se propagent vers le reste du corps, le myélome se caractérise par l’apparition de cellules multiples qui forment des tumeurs à l’intérieur de la moelle osseuse, et sont donc très difficiles à atteindre ».
Le traitement développé par les chercheurs se compose de nanoparticules à base de lipides (similaires à celles utilisées dans le vaccin contre le covid-19) contenant des molécules d’ARN qui réduisent au silence le gène CKAP5, qui code la protéine 5 associée au squelette cellulaire (cytosquelette). Une fois cette protéine inhibée, la cellule cancéreuse est incapable de se diviser, ce qui cause sa mort. Pour éviter d’endommager les cellules saines, les nanoparticules ont été recouvertes d’anticorps qui les guident spécifiquement vers les cellules cancéreuses à l’intérieur de la moelle osseuse.
 Les résultats de l’étude ont été très encourageants : dans des conditions de laboratoire, les cellules étant cultivées dans des flacons, les nanoparticules développées par les chercheurs ont éradiqué près de 90 % des cellules cancéreuses. Dans un deuxième temps, le nouveau traitement a été testé sur des échantillons cancéreux prélevés sur des patients atteints de myélome multiple traités dans le service hémato-oncologique du Centre médical Rabin Medical. Dans ces échantillons, le taux de réussite a été de 60 %. En testant la capacité des nanoparticules à atteindre la moelle osseuse sur des souris de laboratoire, les chercheurs ont constaté que l’ARN pénétrait jusqu’à 60 % des cellules cancéreuses du myélome multiple dans la moelle osseuse après une seule injection, Enfin, l’examen de l’efficacité thérapeutique des nanoparticules sur le modèle murin a montré une éradication des deux tiers des cellules cancéreuses, les souris présentant une amélioration significative de tous les indicateurs cliniques.
Les résultats de l’étude ont été très encourageants : dans des conditions de laboratoire, les cellules étant cultivées dans des flacons, les nanoparticules développées par les chercheurs ont éradiqué près de 90 % des cellules cancéreuses. Dans un deuxième temps, le nouveau traitement a été testé sur des échantillons cancéreux prélevés sur des patients atteints de myélome multiple traités dans le service hémato-oncologique du Centre médical Rabin Medical. Dans ces échantillons, le taux de réussite a été de 60 %. En testant la capacité des nanoparticules à atteindre la moelle osseuse sur des souris de laboratoire, les chercheurs ont constaté que l’ARN pénétrait jusqu’à 60 % des cellules cancéreuses du myélome multiple dans la moelle osseuse après une seule injection, Enfin, l’examen de l’efficacité thérapeutique des nanoparticules sur le modèle murin a montré une éradication des deux tiers des cellules cancéreuses, les souris présentant une amélioration significative de tous les indicateurs cliniques.
Un nouvel horizon thérapeutique
« Les personnes atteintes de myélome multiple souffrent de douleurs osseuses intenses, ainsi que d’anémie, d’insuffisance rénale, et leur système immunitaire s’affaiblit », explique Tarab-Ravski. « Il existe de nombreux traitements possibles de cette maladie, mais après un certain temps d’amélioration, la plupart des patients développent une résistance à la thérapie et la maladie rechute de manière encore plus agressive. Par conséquent, il est constamment nécessaire de développer de nouveaux traitements. La thérapie à base d’ARN présente un grand avantage dans ce cas, car elle peut être développée très rapidement. En effet, on peut inhiber à chaque fois un gène différent en changeant simplement la molécule d’ARN, et ainsi adapter le traitement à la progression de la maladie et à chaque patient individuellement. Le défi de ce type de traitement est d’atteindre les bonnes cellules. Aujourd’hui, les thérapies à base d’ARN sont approuvées pour traiter une certaine maladie génétique du foie et pour les vaccins intramusculaires, comme ça a été le cas pour le covid-19. Le système de délivrement des médicaments que nous avons développé est le premier qui cible spécifiquement les cellules cancéreuses à l’intérieur de la moelle osseuse, et a également été le premier à montrer qu’inhiber l’expression du gène CKAP5 pouvait être un moyen d’exterminer les cellules cancéreuses du sang ».
« Notre technologie ouvre un nouvel horizon pour l’administration sélective de médicaments à base d’ARN et de vaccins contre les tumeurs cancéreuses et les maladies qui trouvent leur originaire dans la moelle osseuse », conclut le Prof. Peer.
L’équipe d’expérimentation clinique comprenait le Dr. Tamar Berger, le Dr. Iuliana Vaxman et le Prof. Pia Raanani de l’Institut d’hématologie du Centre médical Rabin (Hopital Beilinson). L’étude a été financée par le Centre d’hématologie-oncologie Boaz et Varda Dotan de l’Université de Tel-Aviv et par le Lewis Trust pour la recherche sur le cancer du sang.
Photos:
1. Le Prof. Dan Peer (Crédit: Université de Tel-Aviv)
2. Image en couverture de la revue Advanced Science (Crédit: Ella Maru Studio)